歌禮宣佈非酒精性脂肪性肝炎和乙肝領域四篇臨床和臨床前研究摘要入選2021年歐洲國際肝病大會壁報展示
中國杭州和紹興2021年4月12日 /美通社/ -- 歌禮製藥有限公司(香港聯交所代碼:1672)今日宣佈,公司在非酒精性脂肪性肝炎和乙肝領域的四篇臨床和臨床前研究摘要入選2021年歐洲肝臟研究學會(EASL)年會暨國際肝病大會(The International Liver Congress™ 2021, ILC 2021)的壁報展示。以下為4篇摘要的概要信息:
1、標題:肝臟靶向THR-β激動劑ASC41口服片具有顯著降脂作用:一項 Ⅰ 期隨機、雙盲、安慰劑對照單劑量和多劑量遞增研究
摘要/海報編號:1851
類別:非酒精性脂肪性肝病治療
結果:在單劑量遞增的研究中,隨著給藥劑量從1 mg到20 mg,ASC41的藥代動力學特徵呈線性關係,且在高達20 mg的劑量組中仍表現出良好的安全性和耐受性。在多劑量遞增的臨床研究中,經過14天每日口服一次ASC41片劑治療後,給藥組受試者的低密度脂蛋白膽固醇(LDL-C)和甘油三酯(TG)指標相對安慰劑組表現出具有臨床意義和統計學顯著性的降低,如下表所示:
|
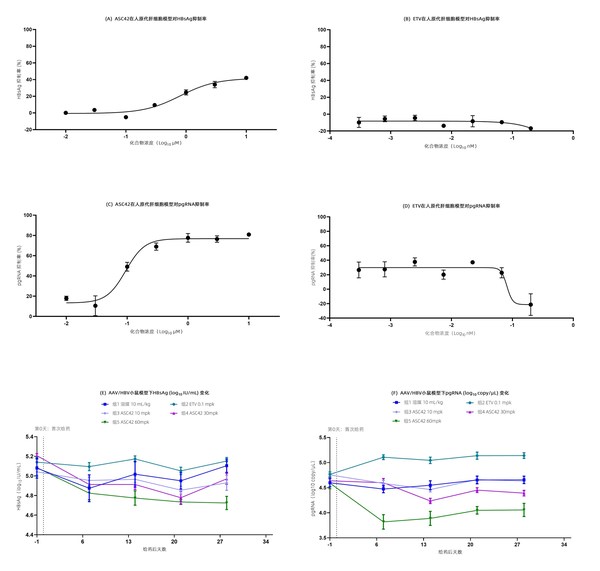
去除安慰劑效應後,經過14天每日口服一次ASC41片劑治療後相對基線變化(平均值) 1 mg (n=12) 2 mg (n=12) 5 mg (n=12) 去除安慰劑效應後,低密度脂蛋白膽固醇(LDL-C)降低 P值 vs 安慰劑 -0.42% P=0.947 -11.94% P=0.052 -19.99% P=0.002 去除安慰劑效應後,甘油三酯(TG)降低 P值 vs 安慰劑 -39.43% P=0.002 -31.06% P=0.029 -34.49% P=0.015 在14天治療中,ASC41在所有劑量組中無3級或以上不良事件、嚴重不良事件或提前停藥事件發生。在14天每日口服一次ASC41片劑的研究中,隨著給藥劑量從1 mg增加到5 mg,ASC41片劑的藥代動力學特徵呈線性關係。 結論:這些數據支持ASC41在非酒精性脂肪性肝炎適應症上開展後期臨床試驗。 2、標題:選擇性THR-β激動劑ASC41對高脂飲食導致患有非酒精性脂肪性肝炎的大鼠非酒精性脂肪性肝活動積分和肝纖維化評分的顯著改善 摘要/海報編號:1908 類別:非酒精性脂肪性肝病治療 結果:ASC41對改善肝脂肪變性、炎性細胞浸潤、氣球樣變和非酒精性脂肪肝活動積分(NAS)呈劑量依賴性。1.5mg/kg和4.5mg/kg劑量的ASC41相比較5mg/kg劑量的MGL3196劑量顯著改善NAS積分,兩者間具有統計學差異。ASC41在0.5mg/kg時,NAS積分降低23.9%,肝纖維化評分降低14.4%,與5 mg/kg時的MGL196相當。ASC41在1.5mg/kg和4.5mg/kg時均顯示出血清低密度脂蛋白的顯著降低。 結論:ASC41對高脂飲食導致患有非酒精性脂肪性肝炎的大鼠可以降低NAS和肝臟纖維化評分。目前的療效數據支持ASC41開展後期臨床試驗。 3、標題:新型非甾體FXR激動劑ASC42對高脂飲食導致的患有非酒精性脂肪性肝炎小鼠非酒精性脂肪性活動積分和肝纖維化評分的顯著改善 摘要/海報編號:1961 類別:非酒精性脂肪性肝病治療 結果:ASC42對改善肝脂肪變性、炎性細胞浸潤、氣球樣變和非酒精性脂肪肝活動積分(NAS)呈劑量依賴性。與30 mg/kg的奧貝膽酸相比,30 mg/kg的ASC42顯示出更高的NAS積分降低(P<0.001)。ASC42在3mg/kg時顯示NAS積分降低46.2%,肝纖維化降低15.2%,與30mg/kg奧貝膽酸相當。在ASC42治療的小鼠中,肝臟中的甘油三酯呈劑量比例下降。 結論:ASC42對高脂飲食導致患有非酒精性脂肪性肝炎的小鼠可以降低NAS積分和肝臟纖維化評分。這些數據支持ASC42開展後期臨床試驗。 4、標題:新型非甾體FXR激動劑ASC42對動物體內和體外HBsAg和HBV pgRNA有顯著抑製作用 摘要/海報編號:1917 類別:病毒性肝炎 結果:在原代人肝細胞(PHH)模型中,對照化合物恩替卡韋(ETV)對HBV DNA具有預期的抑制活性,但對HBV pgRNA和HBsAg無抑製作用,而ASC42對HBsAg、HBV pgRNA和HBV DNA呈劑量依賴性抑制,EC50分別為0.79μM、0.09μM和0.62μM(圖1 A-D)。在AAV/HBV小鼠模型中,ETV(0.1mg/kg)單藥治療後,小鼠血漿HBV DNA明顯下降,HBV pgRNA和HBsAg無明顯下降,ASC42對小鼠血漿中HBV pgRNA、HBsAg、HBV DNA具有劑量依賴性抑製作用。與溶媒對照組相比,ASC42高劑量組(60 mg/kg)分別降低HBV pgRNA、HBsAg和HBV DNA 0.60 log10拷貝/μl(P <0.01)、0.38 log10 IU/μl(P =0.002)和0.77 log10拷貝/μl(P <0.05)(圖1 E-F)。
結論:FXR激動劑ASC42對HBV DNA、HBV pgRNA和HBsAg具有明顯的抑製作用,提示ASC42對乙型肝炎具有臨床治癒的潛力。這一結果支持ASC42在人體中進一步開展臨床試驗。 關於歌禮 歌禮是一家在香港證券交易所上市(1672.HK)的創新研發驅動型生物科技公司。歌禮致力於脂肪性肝炎、腫瘤脂質代謝與口服檢查點抑制劑、病毒性肝炎和艾滋病四大疾病領域創新藥的研發和商業化,滿足國內外患者臨床需求。在具備深厚專業知識及優秀過往成就的管理團隊帶領下,歌禮已發展成為一體化平台型公司,涵蓋了從新藥發現和開發直到生產和商業化的完整價值鏈。 歌禮目前擁有三個商業化產品和十七個在研產品(其中十一個為完全自主研發)。1、非酒精性脂肪性肝炎:歌禮製藥有限公司旗下全資子公司甘萊製藥專注於非酒精性脂肪性肝炎領域創新藥的開發和商業化。甘萊製藥有三款分別針對脂肪酸合成酶(FASN)、甲狀腺激素受體ß(THR-ß)及法尼醇X受體(FXR)的處於臨床階段的候選藥物及三種處於臨床前階段的聯合用藥療法。2、腫瘤脂質代謝與口服檢查點抑制劑:專注於在腫瘤脂質代謝中起關鍵作用的脂肪酸合成酶口服抑制劑管線以及新一代檢查點抑制劑-口服PD-L1小分子抑制劑管線。3、病毒性肝炎:(i) 乙肝:歌禮專注於乙肝臨床治癒創新藥物的研發。探索以皮下注射PD-L1抗體ASC22及派羅欣®為基石藥物,與其他靶點藥物聯合的治療方案,有望為臨床治癒乙肝帶來重大突破。(ii) 丙肝:歌禮成功研發上市兩個1類新藥戈諾衛®和新力萊®,組成全口服丙肝治療方案;ASC18固定劑量復方制劑是升級版的丙肝治療方案,已完成橋接試驗。4、艾滋病:ASC09F是一種用於治療HIV的蛋白酶固定劑量復方抑制劑,ASC09F的臨床試驗申請已獲得批准。欲瞭解更多信息,請登錄網站:www.ascletis.com。
相關鏈接 : http://www.ascletis.com |