
歌禮宣佈在2022年美國肝病研究協會年會以壁報形式報告ASC43F治療NASH的I期單劑量研究
中國杭州和紹興2022年11月7日 /美通社/ -- 歌禮製藥有限公司(香港聯交所代碼:1672,「歌禮」)今日宣佈ASC43F治療非酒精性脂肪性肝炎(NASH)的I期單劑量研究摘要已在2022年美國肝病研究協會(AASLD)年會(The Liver Meeting® 2022)上以壁報形式報告。以下為該摘要的概要信息:
標題:一項旨在評估ASC43F(由甲狀腺激素受體Beta激動劑ASC41和法尼醇X受體激動劑ASC42組成的固定劑量復方制劑口服片)在健康受試者中的安全性、耐受性和藥代動力學的I期單劑量研究
摘要/壁報編號:2314
類別:非酒精性脂肪性肝病治療
研究設計:
ASC43F-101(NCT05118516)是一項在健康受試者中進行的開放標籤、單劑量I期研究。該項研究計劃入組8名18至65歲的受試者,要求男性體重至少50公斤,女性體重至少45公斤,且體重指數(BMI)在18.5-32公斤/平方米(kg/m2)範圍內。兩名符合條件的受試者將先入組。在對這兩名哨點受試者進行為期7天的安全性評估並滿足不停藥的規則後,其餘6名受試者將會入組。
結果:
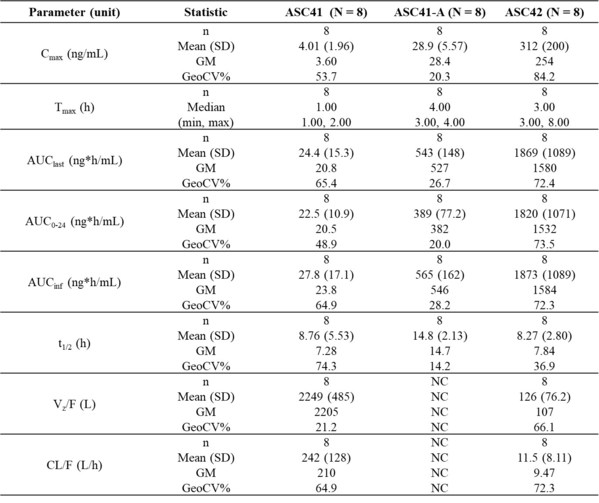
表1:ASC43F中ASC41、ASC41-A和ASC42與單藥治療在健康受試者中的PK參數匯總
結論:
此項I期研究表明,ASC43F顯示出良好的耐受性和安全性,ASC43F中的ASC41/ASC41A和ASC42的藥代動力學(PK)參數與ASC41和ASC42作為單藥治療的PK相似。ASC43F是用於NASH治療的固定劑量復方制劑(FDC),每日用藥一次,每次一片,這將改善患者的依從性。
關於歌禮
歌禮是一家在香港證券交易所上市(1672.HK)的創新研發驅動型生物科技公司,涵蓋了從新藥研發至生產和商業化的完整價值鏈。歌禮的管理團隊具備深厚的專業知識及優秀的過往成就,在團隊的帶領下,歌禮聚焦三大臨床需求尚未滿足的醫療領域:病毒性疾病、非酒精性脂肪肝和腫瘤,並以全球化的視野進行佈局。憑借卓越的執行力,歌禮快速推進藥物管線開發,爭取在國際競爭中佔據領先地位。歌禮目前擁有三個商業化產品,即利托那韋片、戈諾衛® 和新力萊®,以及22款在研藥物。最前沿的候選藥物包括ASC22(乙肝功能性治癒)、ASC10和ASC11(口服小分子抗新冠藥)、ASC40(復發性膠質母細胞瘤)、ASC42(原發性膽汁性膽管炎)和ASC40(痤瘡)。
欲瞭解更多信息,敬請登錄網站:www.ascletis.com。







